Autora: Almudena González Domínguez
El enfoque PICO (Population, Intervention, Comparator, Outcomes) se consolida como la piedra angular del proceso de evaluación clínica, en el nuevo marco europeo de evaluación conjunta de tecnologías sanitarias (Joint Clinical Assessment, JCA).
¿Por qué es tan relevante?
El PICO no es solo una herramienta metodológica clásica de investigación clínica. En el contexto JCA, se convierte en el puente entre las preguntas de política sanitaria de los Estados Miembros y las exigencias de evidencia a los desarrolladores de tecnologías sanitarias o, dicho de otra manera, se convierte en un marco común europeo. Permite que países con sistemas sanitarios distintos trabajen sobre la misma pregunta, dando solidez a los informes conjuntos y credibilidad a las decisiones. Su verdadero valor es la creación de una cultura de evaluación compartida en Europa, donde cada decisión se apoya en evidencia comparable y relevante.
Claves del proceso de definición del PICO en el JCA
1. Partir de las preguntas de política sanitaria: el PICO traduce las necesidades nacionales en preguntas de investigación comparables y estructuradas.
2. Involucrar a todos los Estados Miembros: a través de encuestas PICO, se recogen sus requisitos sobre población, intervención, comparadores y resultados.
3. Integrar perspectivas diversas: no solo autoridades, también pacientes, clínicos y expertos aportan información clave para afinar las definiciones.
4. Consolidar sin perder relevancia: las distintas propuestas nacionales se armonizan en el menor número de PICOs posibles, asegurando que ninguna necesidad quede fuera.
5. Establecer el marco de la evaluación: cada PICO resultante marca qué datos deben solicitarse al desarrollador y cómo se estructurará el informe conjunto.
De la teoría a la práctica
En primavera de 2024, el Subgrupo de la JCA llevó a cabo seis ejercicios piloto PICO: 3 para medicamentos y 3 para productos sanitarios. Estos casos prácticos (disponibles públicamente en la web de la Comisión Europea) muestran cómo la metodología se traduce en escenarios concretos, sirviendo de referencia para futuros procesos.
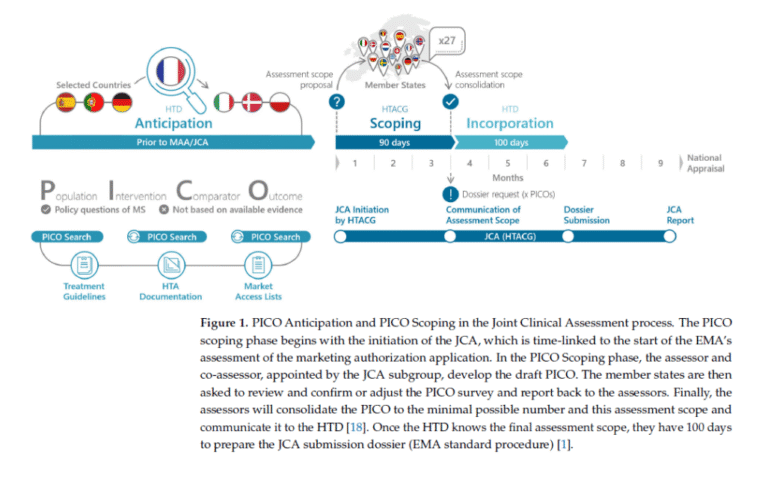
Además, los desarrolladores necesitarán anticipar el PICO en base a información disponible. Dicha información suele provenir de las Agencias de Evaluación, siendo el esquema general de la puesta en marcha según se muestra en la siguiente figura:
Fuente: Eberle K. et al., 2025
Información adicional de interés: PICO vs PECO: Elegir el enfoque adecuado según el tipo de evidencia
Aunque PICO (Population, Intervention, Comparator, Outcomes) es el formato más utilizado en evaluaciones clínicas, especialmente en el marco del Joint Clinical Assessment (JCA) europeo, el enfoque PECO (Population, Exposure, Comparator, Outcomes) resulta más adecuado en estudios observacionales o en contextos donde no hay una intervención activa, sino una exposición natural o ambiental. La diferencia clave radica en el tipo de evidencia que se busca: mientras PICO se centra en ensayos clínicos controlados, PECO permite explorar asociaciones en estudios de cohortes o casos y controles. Esta distinción es relevante porque en la evaluación de tecnologías sanitarias, especialmente productos sanitarios o intervenciones no farmacológicas, puede ser necesario recurrir a evidencia observacional. Reconocer cuándo aplicar PICO o PECO garantiza que las preguntas de evaluación estén alineadas con el tipo de evidencia disponible, mejorando la calidad y la aplicabilidad de los informes conjuntos, y facilitando los posteriores procesos de evaluación y financiación de las tecnologías sanitarias.
Referencias
Cumpston M, Flemyng E. Chapter II: Planning a Cochrane Review [last updated August 2023]. In: Higgins JPT, Thomas J, Chandler J, Cumpston M, Li T, Page MJ, Welch VA, editors. Cochrane Handbook for Systematic Reviews of Interventions version 6.5. Cochrane; 2024. Available from: https://www.cochrane.org/authors/handbooks-and-manuals/handbook/current/chapter-ii
Eberle, K.; Hagemann, L.M.; Schweitzer, M.K.; Justl, M.; Maurer, J.; Carls, A.; Reuter, E.-M. The PICO Puzzle: Can Public Data Predict EU HTA Expectations for All EU Countries? J. Mark. Access Health Policy 2025, 13, 32. https://doi.org/10.3390/jmahp13030032
European Commission. HTA JCA Scoping Process. Brussels: Directorate-General for Health and Food Safety; 2023 [cited 2025 Oct 7]. Available from: https://health.ec.europa.eu/document/download/7be11d76-9a78-426c-8e32-79d30a115a64_en?filename=hta_jca_scoping-process_en.pdf